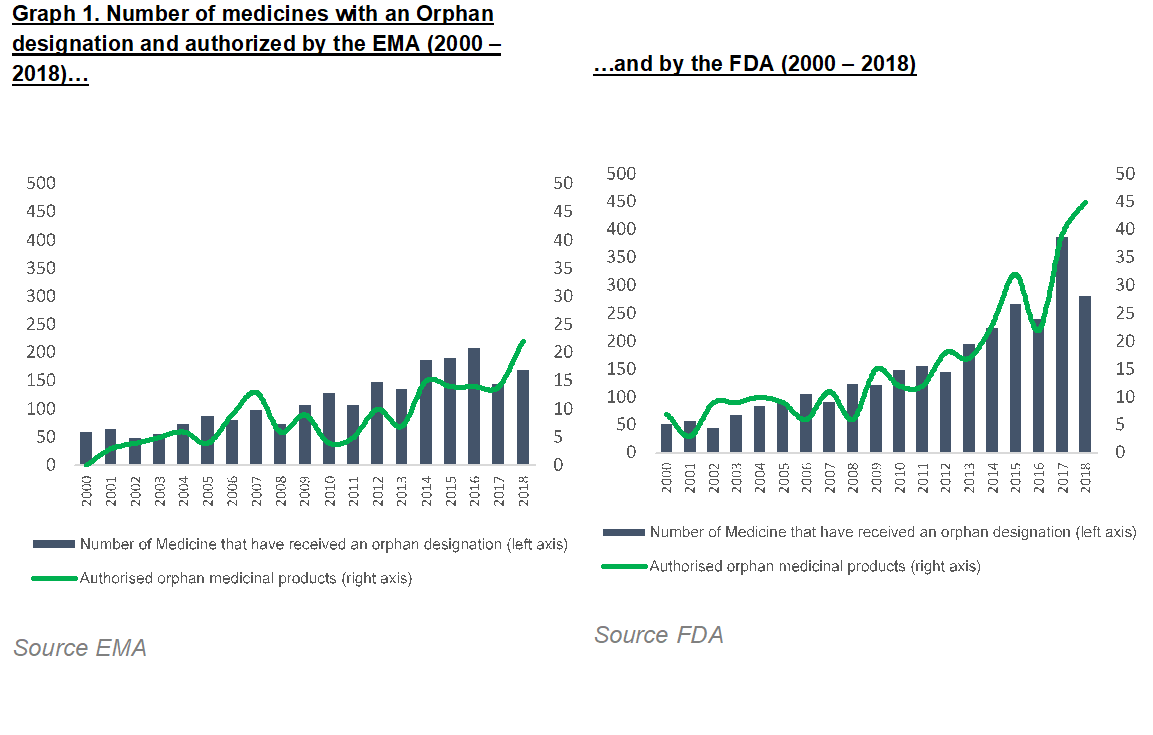
近年来,全球孤儿药临床研发蓬勃发展,方兴未艾。事实上,在2018年,FDA和EMA批准的大多数新药都是孤儿药。
尤其是亚洲国家也开始逐步实施类似于美国《孤儿药法案》的法律框架。包括韩国、中国台湾、新加坡和菲律宾在内的许多国家/地区也在构建这种法律框架。
这些新的亚洲法律框架设定了加快罕见病治疗药物注册和审批的总体标准。标准的制定也为生物制药公司制定了新的医疗保险覆盖范围、加速注册和市场独占期规则。
亚太地区孤儿药临床试验概况
此外,亚太经济合作组织于2018年底启动了《罕见病行动计划》,有望通过各类支持性措施,促进公共服务、疾病登记的发展,帮助患者获得参与临床试验机会,并降低招募患者的用时。
据估计,全球罕见病可能多达8,000余种,约累及全球总人口的6%至8%。欧盟和北美地区约有3000万人罹患罕见病,而亚洲罕见病患者则超过4500万人,其中,仅中国就存在1000万例患者。
最近,中国国家食品药品监督管理总局提出,对已在国外获批的孤儿药,即使没有中国境内的试验数据,也可给予有条件批准。中国也正在积极推进对罕见病和孤儿药的监管。
虽然我们注意到亚洲多个国家出现了相关的法律框架,但由于缺乏跨国家的系统结构,该地区仍然面临挑战。
亚太地区拥有众多治疗领域的关键意见领袖,但缺乏罕见病系统诊断或检测资源。
通过发展患者注册登记可加快孤儿药临床试验的进程。患者病例注册登记是包含健康信息的数据库,用于促进患者参与临床试验,并提供实时上市后监测(包括超说明书用药)。通过注册,监管机构还可以让患者参与药物批准申请评估中相关临床终点的开发。
尽管欧盟有超过700个罕见病登记处,但国际登记处的数量仍然有限。
总而言之,亚洲孤儿药的监管和法律框架构建时间较短,并且各个国家之间又有所不同。但我们观察到近年来该区域促进疾病意识和病例注册登记的举措有所加快。
2018年末,亚太经济合作组织(APEC)启动了《罕见病行动计划》,为协调国内政策、建立最佳实践体系以及加强区域合作提供了框架。
要点
- 我们可以看到,近年来孤儿药的临床开发取得了前所未有的成就。
- 更具体地说,在亚洲,我们看到许多国家加快构建法律框架,这些框架设定了一般标准,以加快罕见病治疗药物的注册和审批速度。
- 亚洲孤儿药的监管和法律框架构建时间较短,并且各个国家之间又有所不同,有些国家仍然缺乏资源,无法对罕见病进行系统诊断或检测。
- 亚太经济合作组织于2018年末启动的《罕见病行动计划》有望通过各类支持性措施,促进公共服务、疾病登记的发展,帮助患者获得参与临床试验机会,并降低招募患者的用时。







